Contoh Soal Ikatan Kovalen: Materi Kimia SMA
Yuk, kuasai materi ikatan kovalen dengan mengerjakan contoh soal berikut ini! Artikel ini akan membahas berbagai jenis soal ikatan kovalen, mulai dari yang sederhana hingga yang lebih kompleks. Sangat cocok untuk siswa SMA yang sedang mempersiapkan diri menghadapi ujian.
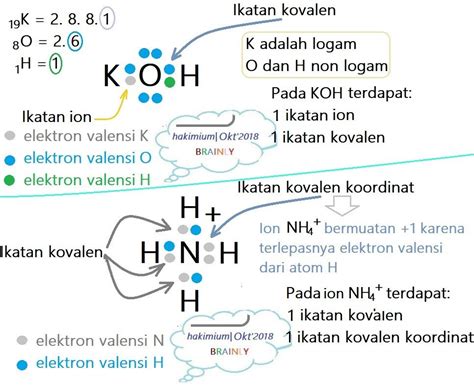
Memahami Ikatan Kovalen
Ikatan kovalen terbentuk melalui pemakaian bersama pasangan elektron antara dua atom. Ikatan ini umumnya terjadi antara atom-atom nonlogam yang memiliki perbedaan elektronegativitas yang relatif kecil. Kekuatan ikatan kovalen bergantung pada jumlah pasangan elektron yang dipakai bersama dan ukuran atom yang terlibat. Mengerti konsep dasar ikatan kovalen sangat penting untuk memahami sifat-sifat senyawa kimia.
Contoh Soal Ikatan Kovalen dan Pembahasannya
Berikut beberapa contoh soal ikatan kovalen beserta pembahasannya:
Soal 1: Jenis Ikatan Kovalen
Jelaskan perbedaan antara ikatan kovalen tunggal, rangkap dua, dan rangkap tiga! Berikan contoh masing-masing!
Pembahasan:
- Ikatan kovalen tunggal: Terbentuk dari satu pasangan elektron yang dipakai bersama. Contoh: H₂ (H-H).
- Ikatan kovalen rangkap dua: Terbentuk dari dua pasangan elektron yang dipakai bersama. Contoh: O₂ (O=O).
- Ikatan kovalen rangkap tiga: Terbentuk dari tiga pasangan elektron yang dipakai bersama. Contoh: N₂ (N≡N).
Soal 2: Struktur Lewis
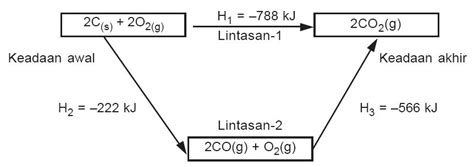
Gambar struktur Lewis untuk molekul CO₂! Tentukan jenis ikatan kovalen yang terdapat dalam molekul tersebut.
Pembahasan:
Struktur Lewis CO₂: O=C=O. Molekul CO₂ memiliki dua ikatan kovalen rangkap dua antara atom karbon dan masing-masing atom oksigen.
Soal 3: Polaritas Ikatan
Manakah di antara molekul berikut yang memiliki ikatan kovalen polar: HCl, Cl₂, H₂? Jelaskan jawaban Anda!
Pembahasan:
Hanya HCl yang memiliki ikatan kovalen polar. Hal ini karena perbedaan elektronegativitas antara atom hidrogen dan klor cukup signifikan, sehingga pasangan elektron tertarik lebih kuat ke atom klor yang lebih elektronegatif. Cl₂ dan H₂ memiliki ikatan kovalen nonpolar karena atom-atom penyusunnya identik, sehingga tidak ada perbedaan elektronegativitas.
Soal 4: Geometri Molekul
Prediksi geometri molekul dari molekul CH₄ menggunakan teori VSEPR!
Pembahasan:
CH₄ memiliki geometri tetrahedral. Atom karbon pusat dikelilingi oleh empat atom hidrogen yang terikat secara kovalen. Teori VSEPR memprediksi bahwa geometri yang paling stabil untuk empat pasangan elektron ikatan adalah tetrahedral dengan sudut ikatan 109,5°.
Tanya Jawab Seputar Ikatan Kovalen
Q: Apa perbedaan utama antara ikatan kovalen dan ikatan ion?
A: Ikatan kovalen melibatkan pemakaian bersama elektron, sedangkan ikatan ion melibatkan transfer elektron. Ikatan kovalen umumnya terjadi antara atom nonlogam, sedangkan ikatan ion terjadi antara logam dan nonlogam.
Q: Bagaimana elektronegativitas memengaruhi sifat ikatan kovalen?
A: Perbedaan elektronegativitas atom-atom yang membentuk ikatan kovalen menentukan polaritas ikatan. Perbedaan elektronegativitas yang besar menghasilkan ikatan kovalen polar, sedangkan perbedaan yang kecil atau nol menghasilkan ikatan kovalen nonpolar.
Q: Apa itu struktur Lewis dan bagaimana cara menggambarnya?
A: Struktur Lewis adalah representasi diagramatik dari distribusi elektron valensi dalam molekul. Cara menggambarnya melibatkan penempatan atom-atom, menghubungkannya dengan garis (pasangan elektron ikatan), dan menempatkan titik-titik (elektron valensi bebas) untuk memenuhi aturan oktet (atau duplet untuk hidrogen). Lebih detailnya, Anda bisa mencari artikel tentang cara menggambar struktur Lewis di website kami! (Link ke artikel terkait - jika ada)
Semoga contoh soal ikatan kovalen di atas bermanfaat untuk membantu Anda memahami materi kimia SMA. Jangan ragu untuk berlatih lebih banyak soal untuk mengasah kemampuan Anda!